Đề thi Học kì 2, Năm học 2022 - 2023, Bài thi môn: Hóa học lớp 11, Có đáp án, (Đề số 5)
Cập nhật: 14/12/2022
Đề thi Học kì 2
Năm học 2022 - 2023
Bài thi môn: Hóa học lớp 11
Thời gian làm bài:45 phút
(không kể thời gian phát đề)
(Đề số 5)
(Cho nguyên tử khối của các nguyên tố: C = 12, O = 16, H = 1, Na = 23, S = 32, K = 39, Ca = 40, Cl = 35,5, N = 14, Cu = 64, Br = 80, Ag = 108)
I. TRẮC NGHIỆM (7 điểm)
Câu 1: Axetilen thuộc dãy đồng đẳng nào?
A. Ankin. B. Anken.
C. Ankan. D. Ankađien.
Câu 2: Ở đáy ấm đun nước dùng lâu ngày thường có một lớp cặn đá vôi. Để loại bỏ lớp cặn này, người ta thường đun ấm với dung dịch
A. giấm ăn. B. muối ăn.
C. nước vôi. D. cồn 70o.
Câu 3: Cho m gam một ancol đơn chức, bậc I đi qua ống chứa CuO đun nóng, sau một thời gian, khối lượng của ống CuO giảm 0,32 gam và thu được hỗn hợp X gồm các chất hữu cơ có tỉ khối so với hiđro là 15,5. Giá trị của m là
A. 0,64. B. 6,2.
C. 1,28. D. 3,1.
Câu 4: Có bao nhiêu đồng phân ankin C5H8 tác dụng được với dung dịch AgNO3/NH3 tạo kết tủa
A. 2. B. 4.
C. 1. D. 3.
Câu 5: Đốt cháy hoàn toàn a mol axit hữu cơ Y được 2a mol CO2. Mặt khác, để trung hòa a mol Y cần vừa đủ 2a mol NaOH. Công thức cấu tạo thu gọn của Y là
A. HOOC-CH2-CH2-COOH.
B. C2H5-COOH.
C. CH3-COOH.
D. HOOC-COOH.
Câu 6: Cho 0,1 mol anđehit X tác dụng với lượng dư AgNO3 (hoặc Ag2O) trong dung dịch NH3, đun nóng thu được 43,2 gam Ag. Hiđro hoá X thu được Y, biết 0,1 mol Y phản ứng vừa đủ với 4,6 gam Na. Công thức cấu tạo thu gọn của X là
A. HCHO.
B. CH3CHO.
C. CH3CH(OH)CHO.
D. OHC-CHO.
Câu 7: Chất nào sau đây được sử dụng để điều chế trực tiếp C2H2 trong phòng thí nghiệm?
A. CaO. B. Al4C3.
C. Al. D. CaC2.
Câu 8: Axit axetic không thể tác dụng được với chất nào?
A. Zn. B. Cu(OH)2.
C. Ag. D. K2CO3.
Câu 9: Điều chế etilen trong phòng thí nghiệm từ C2H5OH, (H2SO4 đặc, 170oC) thường lẫn các oxit như SO2, CO2. Chất dùng để làm sạch etilen là
A. dung dịch KMnO4 loãng dư.
B. dung dịch NaOH dư.
C. dung dịch brom dư.
D. dung dịch Na2CO3 dư.
Câu 10: Cho 2,8 gam anken A làm mất màu vừa đủ dung dịch chứa 8 gam Br2. Hiđrat hóa A chỉ thu được một ancol duy nhất. A có tên là
A. 2-metylpropen.
B. but - 1- en.
C. 2,3-dimetylbut-2-en.
D. but - 2- en.
Câu 11: Để điều chế anđehit từ ancol bằng một phản ứng, người ta dùng
A. ancol bậc I và ancol bậc II.
B. ancol bậc II.
C. ancol bậc III.
D. ancol bậc I.
Câu 12: Để phân biệt but-1-in và but-2-in ta dùng hóa chất gì?
A. dung dịch brom.
B. dung dịch KMnO4.
C. dung dịch AgNO3/NH3.
D. dung dịch HCl.
Câu 13: Đốt cháy hoàn toàn hỗn hợp 3 ankin A, B, C thu được 3,36 lít CO2 (đktc) và 1,8 gam nước. Số mol hỗn hợp ankin bị đốt cháy là
A. 0,15. B. 0,05.
C. 0,08. D. 0,25.
Câu 14: Cho 1,52 gam hỗn hợp gồm hai ancol no, đơn chức, mạch hở là đồng đẳng kế tiếp nhau tác dụng hết với một lượng vừa đủ Na kim loại được 2,18 gam chất rắn. Công thức của hai ancol là công thức nào sau đây?
A. C2H5OH và C3H7OH.
B. C3H7OH và C4H9OH.
C. C4H9OH và C5H11OH.
D. CH3OH và C2H5OH.
Câu 15: Cho các phát biểu sau:
(a) Anđehit vừa có tính oxi hoá vừa có tính khử.
(b) Phenol tham gia phản ứng thế brom khó hơn benzen.
(c) Anđehit tác dụng với H2 (dư) có xúc tác Ni đun nóng, thu được ancol bậc một.
(d) Dung dịch axit axetic tác dụng được với Cu(OH)2.
(e) Dung dịch phenol trong nước làm quỳ tím hoá đỏ.
(g) Trong công nghiệp, axeton được sản xuất từ cumen.
Số phát biểu đúng là
A. 4. B. 3.
C. 5. D. 2.
Câu 16: Dùng H2SO4 đặc, 170oC tách nước 12 gam một ancol no, đơn chức, mạch hở thu được 8,4 gam một anken. Công thức phân tử của ancol đó là
A. C2H5OH.
B. CH3OH.
C. C4H9OH.
D. C3H7OH.
Câu 17: Sắp xếp các chất sau theo chiều giảm dần tính axit: (1) CH3COOH, (2) FCH2COOH, (3) C2H5COOH, (4) ClCH2COOH.
A. (2) > (4) > (1) > (3).
B. (3) > (1) > (4) > (2).
C. (1) > (2) > (3) > (4).
D. (4) > (2) > (3) > (1).
Câu 18: Đốt cháy một hiđrocabon X thu được 2,2 gam CO2 và 1,08 gam H2O. Công thức phân tử của hiđrocacbon X là
A. C6H14. B. C4H10.
C. C5H12. D. C4H8.
Câu 19: Hỗn hợp M gồm một anđehit và một ankin (có cùng số nguyên tử cacbon). Đốt cháy hoàn toàn x mol hỗn hợp M, thu được 3x mol CO2 và 1,8x mol H2O. Phần trăm số mol của anđehit trong hỗn hợp M là
A. 50%. B. 40%.
C. 30%. D. 20%.
Câu 20: Benzen không tham gia phản ứng với
A. H2. B. H2O.
C. Br2. D. O2.
II. TỰ LUẬN (3 điểm)
Câu 1: (1 điểm)
Viết phương trình hóa học hoàn thành chuỗi phản ứng sau:
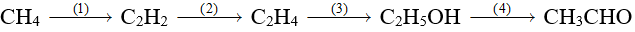
Câu 2: (2 điểm)
Cho 10,1 gam hỗn hợp A gồm 2 ancol no, đơn chức, mạch hở là đồng đẳng kế tiếp nhau tác dụng hết với một lượng natri vừa đủ, thu được 15,6 gam chất rắn và V lít khí hiđro (đktc).
a) Xác định công thức của hai ancol.
b) Tính thành phần phần trăm về khối lượng từng ancol trong hỗn hợp A.
c) Oxi hóa hoàn toàn 5,05 gam hỗn hợp ancol trên bằng CuO, đun nóng. Sau đó, đem toàn bộ sản phẩm hữu cơ cho tác dụng với lượng dư dung dịch AgNO3/NH3 thì thu được a gam Ag↓. Tính a.
--- Hết ---
Giám thị không giải thích thêm
ĐÁP ÁN VÀ HƯỚNG DẪN GIẢI
I. TRẮC NGHIỆM
|
1. A |
2. A |
3. C |
4. A |
5. D |
6. D |
7. D |
8. C |
9. B |
10. D |
|
11. D |
12. C |
13. B |
14. A |
15. A |
16. D |
17. A |
18. C |
19. D |
20. B |
Câu 1:
Đáp án A
Axetilen (C2H2) thuộc dãy đồng đẳng ankin.
Câu 2:
Đáp án A
Ở đáy ấm đun nước dùng lâu ngày thường có một lớp cặn đá vôi. Để loại bỏ lớp cặn này, người ta thường đun ấm với dung dịch giấm ăn vì giấm ăn hòa tan được đá vôi.
2CH3COOH + CaCO3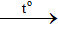 (CH3COO)2Ca + CO2 + H2O
(CH3COO)2Ca + CO2 + H2O
Câu 3:
Đáp án C
Phương trình phản ứng:
RCH2OH + CuO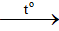 RCHO + Cu + H2O
RCHO + Cu + H2O
⇒ Hỗn hợp X gồm RCHO và RCH2OH dư
Khối lượng chất rắn giảm = mO (oxit) phản ứng
⇒ nO = nCuO =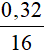 = 0,02 mol
= 0,02 mol
⇒ nanđehit = nCuO = 0,02 mol
Ta có: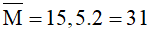
⇒ Hỗn hợp X gồm CH3OH (x mol) và HCHO (0,02 mol)
⇒ 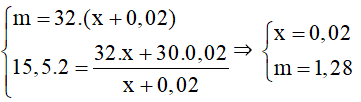
Câu 4:
Đáp án A
Ankin C5H8 tác dụng được với dung dịch AgNO3/NH3 tạo kết tủa.
⇒ Đồng phân ank-1-in.
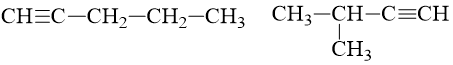
Câu 5:
Đáp án D
Số C =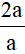 = 2
= 2
Số nhóm chức – COOH =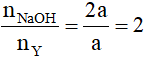
⇒ Công thức cấu tạo của Y là HOOC – COOH.
Câu 6:
Đáp án D
Ta có: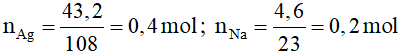
⇒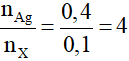 ⇒ X là HCHO hoặc OHC – R – CHO.
⇒ X là HCHO hoặc OHC – R – CHO.
Hiđro hoá X thu được Y ⇒ Y là ancol
0,1 mol Y + 0, 2 mol Na ⇒ Y là ancol 2 chức
⇒ X có dạng OHC – R – CHO.
⇒ OHC – CHO thỏa mãn.
Câu 7:
Đáp án D
CaC2 được sử dụng để điều chế trực tiếp C2H2 trong phòng thí nghiệm.
CaC2 + 2H2O ⟶ C2H2 + Ca(OH)2
Câu 8:
Đáp án C
Axit axetic không thể tác dụng được với Ag.
Câu 9:
Đáp án B
Chất dùng để làm sạch etilen là dung dịch NaOH vì NaOH sẽ hấp thụ CO2 và SO2.
CO2 + 2NaOH ⟶ Na2CO3 + H2O
SO2 + 2NaOH ⟶ Na2SO3 + H2O
Câu 10:
Đáp án D
Gọi công thức phân tử của anken là CnH2n (n ≥ 1)
Ta có:
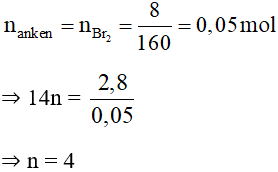
Hiđrat hóa A chỉ thu được một ancol duy nhất ⇒ A là anken đối xứng có 4 nguyên tử C.
⇒ A là but – 2 – en.
Câu 11:
Đáp án D
Để điều chế anđehit từ ancol bằng một phản ứng, người ta dùng ancol bậc I.
RCH2OH + CuO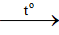 RCHO + Cu + H2O
RCHO + Cu + H2O
Câu 12:
Đáp án C
Để phân biệt but-1-in và but-2-in ta dùng dung dịch AgNO3/NH3 vì but-1-in phản ứng sinh ra kết tủa màu vàng còn but-2-in thì không.
CH ≡ C – CH2 – CH3 + AgNO3 + NH3 ⟶ Ag – C ≡ C – CH2 – CH3↓ + NH4NO3
Câu 13:
Đáp án B
Ta có:
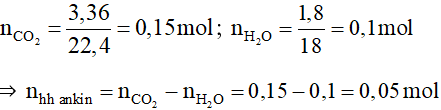
Câu 14:
Đáp án A
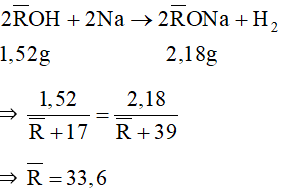
⇒ Công thức của hai ancol là C2H5OH và C3H7OH.
Câu 15:
Đáp án A
a) Đúng.
b) Sai. Phenol có nhóm OH hoạt hóa nhân thơm làm cho phản ứng thế dễ hơn benzen.
c) Đúng.
d) Đúng.
e) Sai. Dung dịch phenol có tính axit nhưng rất yếu, không làm đổi màu quỳ tím.
g) Đúng.
Câu 16:
Đáp án D
Bảo toàn khối lượng ta có:
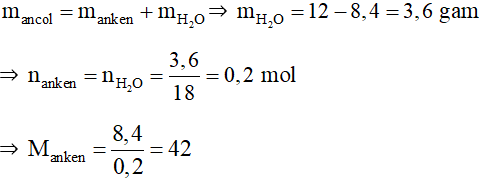
⇒ Anken là C3H6.
⇒ Ancol là C3H7OH.
Câu 17:
Đáp án A
Các nhóm ankyl đẩy electron về phía nhóm caboxyl nên làm giảm lực axit
⇒ Tính axit của CH3COOH > C2H5COOH
Các nguyên tử có độ âm điện lớn như halogen ở gốc R hút electron của nhóm cacboxyl nên làm tính axit tăng.
⇒ Tính axit của CH3COOH < ClCH2COOH < FCH2COOH
⇒ Tính axit giảm dần: (2) > (4) > (1) > (3).
Câu 18:
Đáp án C
Ta có:
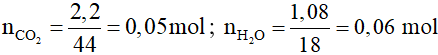
Nhận thấy: ⇒ X là ankan có công thức dạng CnH2n + 2.
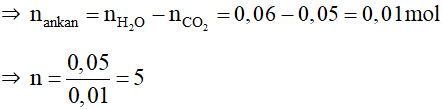
⇒ Công thức phân tử của X là C5H12.
Câu 19:
Đáp án D
Số C của anđehit và ankin là: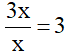
⇒ Ankin là CH ≡ C – CH3 (a mol)
Số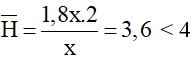
⇒ Anđehit có số C là 3, số H là 2.
⇒ Công thức cấu tạo của anđehit là CH ≡ C – CHO (b mol)
Giả sử x = 1 mol
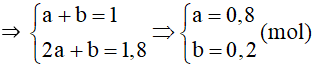
Phần trăm số mol của anđehit trong hỗn hợp M là
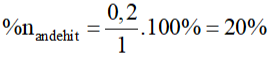
Câu 20:
Đáp án B
Benzen không tác dụng với nước.
II. TỰ LUẬN
Câu 1:
2CH4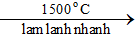 C2H2 + 3H2
C2H2 + 3H2
C2H2 + H2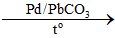 C2H4
C2H4
C2H4 + H2O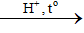 CH3CH2OH
CH3CH2OH
C2H5OH + CuO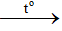 CH3CHO + Cu + H2O
CH3CHO + Cu + H2O
Câu 2:
a) Gọi công thức chung của hai ancol no, đơn chức, mạch hở là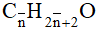
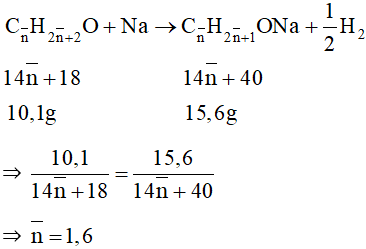
⇒ Công thức của hai ancol đồng đẳng kế tiếp là CH3OH và C2H5OH.
b) Gọi số mol của CH3OH và C2H5OH là a và b (mol).
Theo bài ta có hệ:
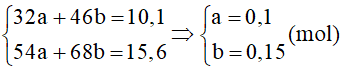
⇒ 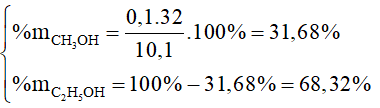
c) Ta có: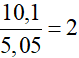
⇒ Trong 5,05 gam hỗn hợp ancol có CH3OH (0,05 mol) và C2H5OH (0,075 mol)
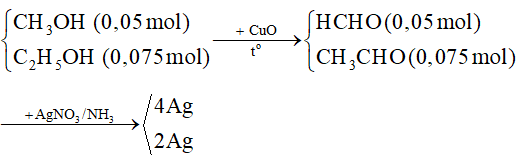
⇒ a = mAg = (0,05.4 + 0,075.2).108 = 27 gam
Nguồn: /

