Đề thi Giữa Học kì 1, Năm học 2022 - 2023, Bài thi môn: Hóa Học lớp 11, Có ma trận, (Đề số 3)
Cập nhật: 14/12/2022
Phần I. Ma trận đề thi giữa học kì 1 hóa 11
|
Nội dung kiến thức
|
Mức độ nhận thức |
Cộng |
||||||||||||
|
Nhận biết |
Thông hiểu |
Vận dụng bậc thấp |
Vận dụng mức cao hơn |
|||||||||||
|
TN |
TL |
TN |
TL |
TN |
TL |
TN |
TL |
|||||||
|
1. Sự điện li
|
- Phân biệt được chất điện li mạnh, chất điện li yếu. - Phân loại chất điện li mạnh yếu, viết phương trình điện li. |
|
- Vận dụng bảo toàn điện tích trong dd các chất điện li |
|
|
|||||||||
|
Số câu hỏi |
2 |
|
|
|
|
|
|
|
2 |
|||||
|
2. Axit - bazơ - muối |
Định nghĩa : axit, bazơ và muối theo thuyết A-rê-ni-ut. Nhận biết hiđroxit lưỡng tính. |
- Phân biệt các loại muối. - Tính nồng độ của dung dịch dung dịch muối khi biết khối lượng. |
|
|
|
|||||||||
|
Số câu hỏi |
1 |
|
1 |
1 |
|
|
|
|
3 |
|||||
|
3. Sự điện li của nước, pH, chất chỉ thị axit - bazơ |
- Định nghĩa môi trường axit và môi trường kiềm dựa vào pH hoặc [H+]
|
- Xác định được môi trường của dung dịch bằng cách sử dụng giấy quỳ tím hoặc pH hoặc [H+] |
- Tính nồng độ H+ dựa vào nồng độ OH- và tích số ion của nước. - Tính pH của dung dịch axit mạnh, bazơ mạnh. |
- Tính pH của dung dịch khi trộn axit mạnh, bazơ mạnh. - Tính pH và kết tủa. |
|
|||||||||
|
Số câu hỏi |
1 |
|
1 |
|
|
1 |
|
1 |
4 |
|||||
|
4. Phản ứng trao đổi ion trong dung dịch các chất điện li |
- Bản chất phản ứng trao đổi ion - Điều kiện xảy ra phản ứng trao đổi ion. |
- Viết được phương trình phân tử và ion rút gọn. - Xác định các cặp chất xảy ra phản ứng hoặc không xảy ra phản ứng.
|
|
- Bài tập tổng hợp về phương trình ion rút gọn. - Các bài tập hiddroxit lưỡng tính, oxit axit pứ với dd kiềm, dd H+ pứ muối cacbonat |
|
|||||||||
|
Số câu hỏi |
1 |
|
1 |
1 |
|
|
|
|
3 |
|||||
|
5. Nito- photpho |
- Nêu được cấu tạo nguyên tử, phân tử, tính chất vật lí, hóa học, trạng thái tự nhiên, điều chế, ứng dụng của nitơ và hợp chất của nito |
- Viết được ptpư thể hiện tchh của nitơ và các hợp chất của nitơ. - Nêu hiện tượng và giải thích. - Xác định được vai trò của các chất trong một phản ứng (oxi hóa khử) cụ thể. - Xác định các cặp chất có phản ứng với nhau được hay không. |
- Giải bài toán liên quan đến amoniac, muối amoni, muối nitrat. - Giải bài toán phản ứng của kim loại, oxit kim loại với dung dịch HNO3. - Tổng hợp lý thuyết về nitơ và các hợp chất của nitơ. |
- Giải quyết vấn đề thực tiễn, thực nghiệm có liên quan đến nitơ và hợp chất của nó. - Giải được bài toán liên quan đến phản ứng điều chế amoniac, bài toán KL với HNO3. |
|
|||||||||
|
2 |
1 |
2 |
1 |
4 |
1 |
1 |
1 |
13 |
||||||
|
Tổng |
7 |
1 |
5 |
3 |
4 |
2 |
1 |
2 |
25 |
|||||
PHẦN II. ĐỀ THI
Đề thi Giữa Học kì 1
Năm học 2022 - 2023
Bài thi môn: Hóa Học lớp 11
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
(Đề số 3)
Câu 1: Một dung dịch có [H+] < [OH-] thì dung dịch đó có môi trường
A. axit.
B. bazơ.
C. trung tính.
D. không xác định được.
Câu 2: Phương trình điện li nào sau đây không đúng?
A. H2SO4 → 2H+ + SO42- .
B. CH3COOH ⇌ CH3COO- + H+ .
C. HF → H+ + F-.
D. KClO → K+ + ClO- .
Câu 3: Dung dịch nào sau đây không dẫn điện?
A. Dung dịch HCl trong nước.
B. Dung dịch glucozơ trong nước.
C. Dung dịch NaCl trong nước.
D. Dung dịch NaOH trong nước.
Câu 4: Theo thuyết Areniut, phát biểu nào sau đây đúng?
A. Axit axetic (CH3COOH) là axit nhiều nấc.
B. Một hợp chất trong thành phần phân tử có hiđro là axit.
C. Bazơ là chất khi tan trong nước phân li ra ion OH-.
D. Một hợp chất trong thành phần phân tử có nhóm OH là bazơ.
Câu 5: Các ion nào sau đây cùng tồn tại trong một dung dịch?
A. Na+, Mg2+, NO3-, PO43-.
B. Ba2+, Na+, Cl-, HCO3-.
C. Ag+, Fe2+, HCO32-, NO3-.
D. K+, Al3+, Cl-, CO32-.
Câu 6: Phản ứng nào sau đây là phản ứng trao đổi ion trong dung dịch chất điện li?
A. CaO + CO2 → CaCO3.
B. Fe + CuCl2 → FeCl2 + Cu.
C. Ba(NO3)2 + 2NaOH → Ba(OH)2 + 2NaNO3.
D. MgSO4 + Ca(OH)2 → Mg(OH)2 + CaSO4.
Câu 7: Dung dịch gồm NaOH 0,2M và Ba(OH)2 0,1M có giá trị pH là
A. 13,6.
B. 0,4.
C. 0,5.
D. 13,5.
Câu 8: Chất X là muối khi tan trong nước tạo ra dung dịch có môi trường axit. Khi cho X tác dụng với dung dịch BaCl2 dư hay dung dịch KOH dư đều thu được kết tủa (sau khi phản ứng xảy ra hoàn toàn). X là
A. Al2(SO4)3.
B. ZnSO4.
C. Na2SO4.
D. CuSO4.
Câu 9: Trong dung dịch H3PO4 có tất cả bao nhiêu anion (bỏ qua sự phân li của nước)?
A. 1.
B. 2.
C. 3.
D. 4.
Câu 10: Muối nào sau đây là muối axit?
A. NH4HCO3.
B. HCOONa.
C. HCOONH4.
D. (NH4)2CO3.
Câu 11: Cho các chất sau: K2CO3; (NH4)2CO3; Al(OH)3; Fe(OH)2; Zn(OH)2; Ag; Cr(OH)3; Cu(OH)2; Al; Zn; CuS. Số chất tác dụng được với HCl là
A. 8.
B. 10.
C. 9.
D. 7.
Câu 12: Trong số các chất sau: HNO2, CH3COOH, C6H6, HCOOH, C6H12O6, C2H5OH, NaClO, CH4, NaOH, NH4NO3 , H2S. Số chất thuộc loại chất điện li yếu là
A. 7.
B. 5.
C. 6.
D. 4.
Câu 13: Cho các dung dịch có cùng nồng độ 0,01M: Ba(OH)2 (1); H2SO4 (2); NaOH (3); Na2SO4 (4). Thứ tự giảm dần giá trị pH của các dung dịch đó là
A. (2), (4), (3), (1).
B. (1), (3), (4), (2).
C. (1), (3), (2), (4).
D. (2), (3), (4), (1).
Câu 14: Xác định chất (A) và (B) trong chuỗi sau :
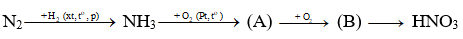
A. (A) là NO, (B) là N2O5 B. (A) là NO, (B) là NO2
C. (A) là N2, (B) là N2O5 D. (A) là N2, (B) là NO2
Câu 15: Cho các phản ứng hóa học sau:
(1) (NH4)2SO4 + BaCl2→ (2) CuSO4 + Ba(NO3)2→
(3) Na2SO4 + BaCl2→ (4) H2SO4 + BaSO3→
(5) (NH4)2SO4 + Ba(OH)2→ (6) Fe2(SO4)3 + Ba(NO3)2→
Các phản ứng đều có cùng một phương trình ion rút gọn là:
A. (1), (2), (3), (6). B. (1), (3), (5), (6).
C. (2), (3), (4), (6). D. (3), (4), (5), (6).
Câu 16: Tiến hành các thí nghiệm sau:
(1) Sục khí SO2 vào dung dịch H2S.
(2) Sục khí NH3 tới dư vào dung dịch AlCl3.
(3) Cho mẩu Na vào dung dịch CuSO4.
(4) Sục khí CO2 tới dư vào dd Ca(OH)2
(5) Cho dung dịch AgNO3 vào dung dịch NaCl.
(6) Sục khí H2S tới dư vào dd Pb(NO3)2
Sau khi các phản ứng kết thúc, có bao nhiêu thí nghiệm thu được kết tủa?
A. 3. B. 5. C. 4. D. 2.
Câu 17: Hòa tan các chất sau: KOH, C2H5OH, C12H22O11, NaCl vào nước để thu được các dung dịch riêng rẽ. Trong các dung dịch thu được, có bao nhiêu dung dịch có khả năng dẫn điện?
A. 3 B. 2 C. 5 D. 6
Câu 18: Phương trình phản ứng nào dưới đây có phương trình ion rút gọn là:
H+ + OH- → H2O :
A. NH4Cl + NaOH→ NH3 + H2O + NaCl
B. Mg(OH)2 + 2HNO3→ Mg(NO3)2+ 2H2O
C. NaOH + HNO3 → NaNO3 + H2O
D. Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
Câu 19: Cho 1,86 gam hỗn hợp Al và Mg tác dụng với dung dịch HNO3 loãng dư, thu được 560 ml lít khí N2O (đktc, sản phẩm khử duy nhất) bay ra. Khối lượng muối nitrat tạo ra trong dung dịch là
A. 40,5 gam. B. 14,62 gam.
C. 24,16 gam. D. 14,26 gam.
Câu 20: Có 4 dung dịch không màu: NH4Cl, (NH4)2SO4, BaCl2, Na2CO3 đựng trong 4 lọ mất nhãn riêng biệt. Dùng một dung dịch thuốc thử dưới đây để phân biệt 4 lọ trên
A. NaCl. B. NH3. C. NaNO3. D. Ba(OH)2.
Câu 21: Dãy các chất đều tác dụng với dung dịch Ba(OH)2 là:
A. NaHCO3, Na2CO3, CO2, MgSO4 , HCl
B. Mg(NO3)2, HCl, BaCl2, NaHCO3, Na2CO3
C. NaHCO3, Na2CO3, CO2, Mg(NO3)2, Ba(NO3)2
D. Ba(NO3)2, Mg(NO3)2, HCl, CO2, Na2CO3.
Câu 22: Cho V lít (đktc) hỗn hợp N2 và H2 có tỷ lệ mol 1:4 vào bình kín và đun nóng. Sau phản ứng được 1,5 mol NH3. Biết hiệu suất phản ứng là H = 25%. Giá trị của V là
A. 42 lít B. 268,8 lít C. 336 lít D. 448 lít
Câu 23: Nhỏ từ từ từng giọt cho đến hết 200 ml dung dịch HCl 0,5M và HNO3 0,5M vào 100 ml dung dịch X chứa hỗn hợp gồm Na2CO3 1,5M và KHCO3 1M, thu được V lít khí CO2 (ở đktc). Giá trị của V là
A. 1,12.
B. 2,24.
C. 3,36.
D. 4,48.
Câu 24: Dung dịch X gồm 0,15 mol K+; 0,3 mol Mg2+; 0,25 mol Na+; a mol Cl- và b mol SO42-. Cô cạn dung dịch X thu được 61,8 gam muối khan. Giá trị của b là
A. 0,4.
B. 0,3.
C. 0,2.
D. 0,5.
Câu 25: Nung 2,23 gam hỗn hợp X gồm các kim loại Fe, Al, Zn, Mg trong oxi, sau một thời gian thu được 2,71 gam hỗn hợp Y. Hoà tan hoàn toàn Y vào dung dịch HNO3(dư), thu được 0,672 lít khí NO (sản phẩm khử duy nhất, ở đktc). Số mol HNO3 đã phản ứng
A. 0,12. B. 0,14. C. 0,16. D. 0,18.
Nguồn: /

