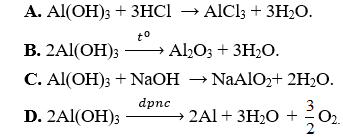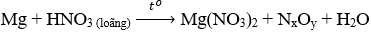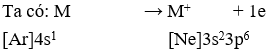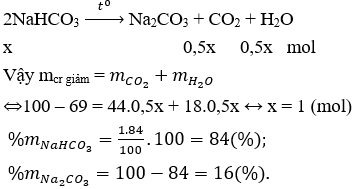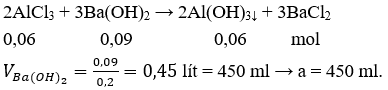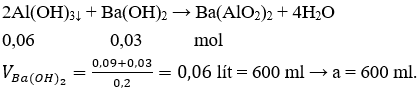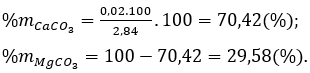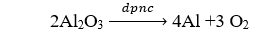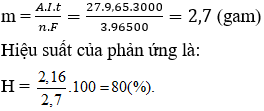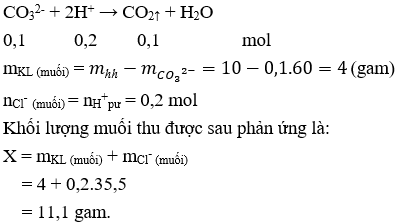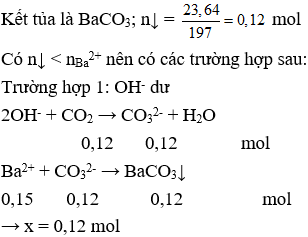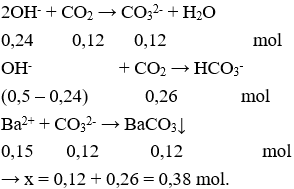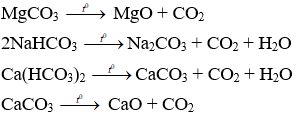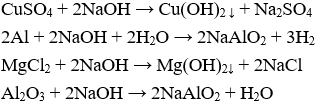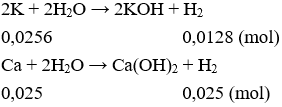Đề thi Giữa học kì 2, Môn: Hóa Học 12, (Đề 3)
Cập nhật: 14/12/2022
Đề thi Giữa học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 3)
Câu 1. Cation M+ có cấu hình electron ở lớp ngoài cùng là 3s23p6. M+ là cation
A. Ag+.
B. Cu+.
C. Na+.
D. K+.
Câu 2. Tính chất không phải của kim loại kiềm là
A. Có nhiệt độ nóng chảy thấp nhất trong tất cả kim loại.
B. Có số oxi hoá +1 trong các hợp chất.
C. Kim loại kiềm có tính khử mạnh.
D. Độ cứng cao.
Câu 3. Nung 100g hỗn hợp gồm Na2CO3 và NaHCO3 cho đến khi khối lượng của hỗn hợp không đổi được 69g chất rắn. Thành phần % theo khối lượng của Na2CO3 và NaHCO3 lần lượt là
A. 84% ; 16%.
B. 16% ; 84%.
C. 32% ; 68%.
D. 68% ; 32%.
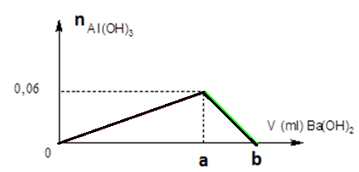
Câu 4: Rót từ từ dung dịch Ba(OH)2 0,2M vào 150 ml dung dịch AlCl3 0,4M thấy lượng kết tủa phụ thuộc vào số ml dung dịch Ba(OH)2 theo đồ thị dưới đây
Giá trị của a và b tương ứng là:
A. 450 ml và 600 ml.
B. 450 ml và 900 ml.
C. 900 ml và 120 ml.
D. 600 ml và 900 ml.
Câu 5. Cho 2,84g hỗn hợp CaCO3 và MgCO3 tác dụng hết với dung dịch HCl thu được 0,03 mol khí CO2. Thành phần % theo khối lượng của CaCO3 và MgCO3 trong hỗn hợp lần lượt là
A. 70,4% và 29,6%.
B. 29,6% và 70,4%.
C. 59,15% và 40,85%.
D. 40,85% và 59,15%.
Câu 6. Kim loại thuộc nhóm IIA không tác dụng với nước ngay cả ở nhiệt độ cao là
A. Be.
B. Mg.
C. Ca.
D. Ba.
Câu 7. Xếp các kim loại kiềm thổ theo chiều tăng dần của điện tích hạt nhân, thì
A. bán kính nguyên tử giảm dần.
B. khối lượng riêng giảm dần.
C. tính khử giảm dần.
D. khả năng tác dụng với nước tăng dần.
Câu 8. Phân biệt dung dịch Ca(HCO3)2 với dung dịch CaCl2 bằng
A. Dung dịch HCl.
B. Dung dịch Na2CO3.
C. Dung dịch Na3PO4.
D. Dung dịch NaCl.
Câu 9. Dung dịch làm mềm nước cứng tạm thời và vĩnh cửu là
A. Ca(OH)2.
B. HCl.
C. Na2CO3
D. NaNO3.
Câu 10. Ion Al3+ bị khử trong trường hợp
A. Điện phân dung dịch AlCl3 với điện cực trơ có màng ngăn.
B. Điện phân Al2O3 nóng chảy.
C. Dùng H2 khử Al2O3 ở nhiệt độ cao.
D. Thả Na vào dung dịch Al2(SO4)3.
Câu 11. Phương trình phản ứng hoá học chứng minh Al(OH)3 có tính axit là
Câu 12. Chọn câu không đúng
A. Nhôm là kim loại nhẹ, dẫn điện, dẫn nhiệt tốt.
B. Nhôm có tính khử mạnh chỉ sau kim loại kiềm và kiềm thổ.
C. Nhôm bị phá hủy trong môi trường kiềm.
D. Nhôm là kim loại lưỡng tính.
Câu 13. Trong những chất sau, chất dẫn điện tốt nhất là
A. Al.
B. Ag.
C. Cu.
D. Fe.
Câu 14. Điện phân Al2O3 nóng chảy với dòng điện cường độ 9,65A trong thời gian 3000 giây thu được 2,16g Al. Hiệu suất điện phân là
A. 60%.
B. 70%.
C. 80%.
D. 90%.
Câu 15. Hoà tan hết 10g hỗn hợp muối cacbonat của kim loại IA và IIA bằng dung dịch HCl dư, thu được 2,24 lít khí (đktc). Sau đó cô cạn dung dịch thu được x gam muối khan. x có giá trị là
A. 12,00g.
B. 11,10g.
C. 11,80g.
D. 14,20g.
Câu 16. Hoà tan hết 3,5g hỗn hợp kim loại gồm Mg, Al và Fe bằng dung dịch HCl dư, thu được 3,136 lít khí (đktc) và dung dịch chứa m gam muối clorua. m nhận giá trị bằng
A. 13,44g.
B. 15,2g.
C. 9,6g.
D. 12,34g.
Câu 17. chất nào sau đây không tan trong HNO3 đặc nguội?
A. CuO.
B. Cu.
C. Al.
D. ZnO.
Câu 18. Cho x mol CO2 hấp thụ hoàn toàn vào 200ml dung dịch hỗn hợp gồm KOH 1M và Ba(OH)2 0,75M thu được 23,64g kết tủa. Giá trị của x là
A. 0,12 hoặc 0,38.
B. 0,12.
C. 0,88.
D. 0,12 hoặc 0,90.
Câu 19. Bằng phương pháp hóa học, để phân biệt các dung dịch riêng biệt: K2SO4, MgCl2, AlCl3, có thể chỉ dùng một dung dịch là
A. AgNO3.
B. BaCl2.
C. KOH.
D. HNO3.
Câu 20. Phát biểu nào sau đây là đúng?
(1) Na2CO3 được ứng dụng để sản xuất thủy tinh, bột giặt, ...
(2) NaCl được dùng làm thuốc muối chữa bệnh dạ dày, bột nở.
(3) NaOH được ứng dụng trong chế biến dầu mỏ và sản xuất xà phòng, ...
(4) CaSO4.2H2O được sử dụng làm vật liệu xây dựng, sản xuất: amoniac, clorua vôi, ...
(5) Mg được ứng dụng sản xuất hợp kim nhẹ, chất tạo màu trắng trong pháo hoa, ...
A. (1), (3), (5).
B. (1), (2), (3), (4).
C. (2), (3), (5).
D. (3), (4), (5).
Câu 21.Dãy các chất đều bị nhiệt phân là
A. MgCO3, NaHCO3, CaCO3, Ca(HCO3)2.
B. CaCO3, Ca(HCO3)2, Al(OH)3, Na2CO3.
C. Ca(HCO3)2, Al(OH)3, Al2O3.
D. CaO, Ca(HCO3)2, Al(OH)3, NaHCO3.
Câu 22:Dãy chất phản ứng với dung dịch NaOH là
A. Mg(OH)2, Al2O3, Al(OH)3.
B. CuSO4, Al, MgCl2, Al2O3.
C. Cu(NO3)2, CuSO4, Mg(OH)2, Al2O3.
D. CuSO4, KOH, Mg(OH)2, Al2O3.
Câu 23.Dãy chất đều phản ứng với HNO3 đặc, nguội là
A. Mg, Ca, Al, Fe, Zn.
B. Mg, K, Al, Cu, Zn.
C. Fe, Cu, Mg, Zn, K.
D. Mg, Cu, K, Zn, Ca,
Câu 24. Chất nào sau đây được gọi là đá vôi?
A. CaCO3.
B. Ca(OH)2.
C. CaO.
D. CaSO4.
Câu 25. Khuấy đều một lượng bột Fe và Fe3O4 vào dung dịch HNO3 loãng. Chấm dứt phản ứng thu được dung dịch X, NO và còn dư Fe. Dung dịch X chứa chất tan
A. Fe(NO3)2.
B. Fe(NO3)2 và Fe(NO3)3.
C. Fe(NO3)3 và HNO3.
D. Fe(NO3)2, Fe(NO3)3, HNO3.
Câu 26: Khi hòa tan hoàn toàn m gam mỗi kim loại vào nước dư, từ kim loại nào sau đây thu được thể tích khí H2 (cùng điều kiện nhiệt độ và áp suất) là nhỏ nhất?
A. Na.
B. Ca.
C. K.
D. Li.
Câu 27: Loại đá và khoáng chất nào sau đây không chứa canxi cacbonat?
A. Đá hoa cương.
B. Thạch cao.
C. Đá phấn.
D. Đá vôi.
Câu 28: Cho phản ứng:
Sau khi cân bằng, hệ số của phân tử HNO3 là
A. 5x – 2y.
B. 12x – 4y.
C. 10x – 4y.
D. 2x – 4y.
Câu 29: Cho 2,16 gam Mg tác dụng với dung dịch HNO3 (dư). Sau khi phản ứng xảy ra hoàn toàn thu được 0,896 lít khí NO (ở đktc) và dung dịch X. Khối lượng muối khan thu được khi làm bay hơi dung dịch X là
A. 13,32 gam.
B. 6,52 gam.
C. 8,88 gam.
D. 13,92 gam.
Câu 30: Phát biểu nào sau đây là sai ?
A. Điều kiện để một kim loai A đẩy kim loại B ra khỏi muối là A phải mạnh hơn B.
B. Nguyên tử kim loại chỉ có tính khử, không có tính oxi hóa.
C. Kim loại có độ cứng lớn nhất là Cr.
D. Trạng thái cơ bản, kim loại kiềm thổ có số electron hóa trị là 2.
Đáp án & Thang điểm
Câu 1. D
Vậy M là Kali.
Câu 2. D
Kim loại kiềm có độ cứng thấp.
Câu 3. B
Nung hỗn hợp chỉ có NaHCO3 bị phân hủy.
Câu 4. A
Tại thời điểm VBa(OH)2 = a (ml) kết tủa đạt cực đại
Tại thời điểm VBa(OH)2 = b (ml) kết tủa tan hoàn toàn
Câu 5. A
Gọi số mol của CaCO3 và MgCO3 lần lượt là x và y (mol)
nhh = 2,84 gam → 100x + 84y = 2,84 (1)
Bảo toàn C có: x + y = nCO2 = 0,03 (2)
Từ (1) và (2) có x = 0,02 và y = 0,01.
Câu 6. A
Be không tác dụng với nước, ngay cả nhiệt độ cao.
Câu 7. D
Ở nhiệt độ thường, Be không tác dụng với nước; Mg tác dụng chậm với nước; các kim loại còn lại tác dụng mạnh với nước giải phóng H2.
Câu 8. A
Ca(HCO3)2 + 2HCl → CaCl2 + 2CO2 ↑ + 2H2O
CaCl2 + HCl → không phản ứng.
Câu 9. C
Mg2+ + CO32- → MgCO3↓
Ca2+ + CO32- → CaCO3↓
Câu 10. B
Câu 11. C
Al(OH)3 thể hiện tính axit qua phản ứng với dung dịch kiềm.
Câu 12. D
Không có khái niệm kim loại lưỡng tính.
Câu 13. B
Ag dẫn điện tốt nhất.
Câu 14. C
Khối lượng nhôm thu được theo lý thuyết là:
Câu 15. B
Câu 16. A
Bảo toàn H có: nHCl = 2.nkhí = 0,28 (mol)
Bảo toàn khối lượng có: m = mKL + maxit pư - mkhí = 3,5 + 0,28.36,5 – 0,14.2 = 13,44 (gam).
Câu 17. C
Al bị thụ động trong HNO3 đặc, nguội.
Câu 18. A
nOH- = 0,2.1 + 0,2.2.0,75 = 0,5 (mol)
nBa2+ = 0,2.0,75 = 0,15 (mol)
Trường hợp 2: Sau phản ứng thu được HCO3- và CO32-
Câu 19. C
Dùng dung dịch KOH.
+ Xuất hiện kết tủa trắng → MgCl2.
+ Xuất hiện kết tủa keo trắng, tan trong KOH dư → AlCl3.
+ Không hiện tượng: K2SO4.
Câu 20. A
Phát biểu đúng là:
(1) Na2CO3 được ứng dụng để sản xuất thủy tinh, bột giặt, ...
(3) NaOH được ứng dụng trong chế biến dầu mỏ và sản xuất xà phòng, ...
(5) Mg được ứng dụng sản xuất hợp kim nhẹ, chất tạo màu trắng trong pháo hoa, ...
Câu 21. A
Câu 22. B
Câu 23. D
Loại A, B và C do Al, Fe thụ động trong HNO3 đặc, nguội.
Câu 24. A
Thành phần chính của đá vôi: CaCO3.
Câu 25. A
Sau phản ứng còn dư Fe nên dung dịch X chỉ chứa Fe(NO3)2.
Câu 26: C
So sánh nhóm I: Li, Na, K.Ta có MK lớn nhất → Vkhí thu được là nhỏ nhất.
Giả sử m = 1 gam.
Câu 27: B
Thạch cao không chứa canxi cacbonat (thành phần chính của thạch cao là CaSO4).
Câu 28: B.
(5x – 2y)Mg + (12x – 4y)HNO3 (loãng) (t°)→ (5x – 2y)Mg(NO3)2 + 2NxOy + (6x – 2y) H2O
Câu 29. D
Bảo toàn e: nMg.2 = 0,18 > nNO.3 = 0,12.
Vậy sản phẩm khử còn NH4NO3: 0,0075 mol.
mmuối = mMg(NO3)2 + mNH4NO3 = 0,09.148 + 0,0075.80 = 13,92g.
Câu 30. A
Điều kiện để một kim loai A đẩy kim loại B ra khỏi dung dịch muối là A phải mạnh hơn B và A không tác dụng được với nước.
Nguồn: /
Tags : Đề thi Giữa học kì 2 Hóa Học 12 Đề 3