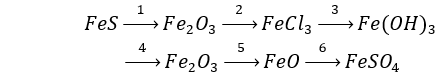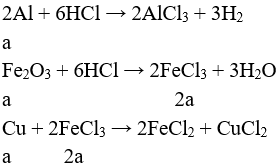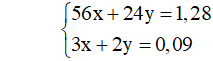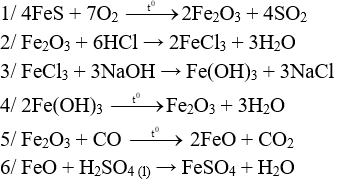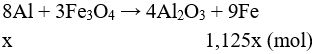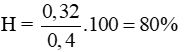Đề thi Giữa học kì 2, Môn: Hóa Học 12, Trắc nhiệm, Tự luận, (Đề 7)
Cập nhật: 14/12/2022
Đề thi Giữa học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 7)
Cho nguyên tử khối của các nguyên tố: C = 12, H = 1, O = 16, Fe = 56, Cr = 52, Mg = 24, Al = 27.
I. Phần trắc nghiệm
Câu 1: Hỗn hợp X gồm Al, Fe2O3, Cu có số mol bằng nhau. Hỗn hợp X tan hoàn toàn trong
A. AgNO3 dư.
B. NH3 dư.
C. NaOH dư.
D. HCl dư.
Câu 2: Chọn câu đúng ?
A. Khi thêm dung dịch bazơ vào muối cromat màu vàng sẽ tạo thành đicromat có màu da cam.
B. Khi thêm dung dịch axit vào muối cromat màu vàng sẽ tạo thành đicromat có màu da cam.
C. Khi thêm dung dịch axit vào muối cromat màu da cam sẽ tạo thành đicromat có màu vàng.
D. Khi thêm dung dịch bazơ vào muối cromat màu da cam sẽ tạo thành đicromat có màu vàng.
Câu 3: Cation M3+ có cấu hình electron ở lớp ngoài cùng là 2s22p6. Vị trí M trong bảng tuần hoàn là
A. ô 13, chu kì 3, nhóm IIIA.
B. ô 13, chu kì 3, nhóm IIIB.
C. ô 13, chu kì 3, nhóm IA.
D. ô 13, chu kì 3, nhóm IB.
Câu 4: Có các kim loại Cu, Ag, Fe và các dung dịch muối Cu(NO3)2, Fe(NO3)3, AgNO3 . Kim loại nào tác dụng được với cả 3 dung dịch muối?
A. Cu.
B. Ag .
C. Fe.
D. Cu, Fe.
Câu 5: Chọn câu không đúng
A. Nhôm là kim loại nhẹ, dẫn điện, dẫn nhiệt tốt.
B. Nhôm có tính khử mạnh chỉ sau kim loại kiềm và kiềm thổ.
C. Nhôm bị phá hủy trong môi trường kiềm.
D. Nhôm là kim loại lưỡng tính.
Câu 6: Quặng nhôm (nguyên liệu chính) được dùng trong sản xuất nhôm là
A. Boxit Al2O3.2H2O.
B. Criolit Na3AlF6 (hay 3NaF.AlF3).
C. Aluminosilicat (Kaolin) Al2O3.2SiO2.2H2O.
D. Mica K2O.Al2O3.6SiO2.2H2O.
Câu 7: Cần bao nhiêu tấn quặng manhetit chứa 80% Fe3O4 để có thể luyện được 800 tấn gang có hàm lượng 95%. Lượng Fe hao hụt trong sản xuất là 1%.
A. 2351,16 tấn.
B. 3512,61 tấn.
C. 1325,16 tấn.
D. 5213,61 tấn.
Câu 8: Cho 5,2 gam Cr tác dụng với HNO3 loãng dư, thu được V lít khí NO (sản phẩm khử duy nhất ở đktc). V có giá trị là
A. 3,36.
B. 6,72.
C. 4,48.
D. 2,24.
Câu 9: Hoà tan hoàn toàn 1,28 gam hỗn hợp Fe và Mg trong lượng dư dung dịch HNO3 thấy thoát ra 0,03 mol khí NO duy nhất (đktc). Số mol Fe và Mg trong hỗn hợp lần lượt là
A. 0,01 mol và 0,03 mol.
B. 0,02 mol và 0,03 mol.
C. 0,03 mol và 0,02 mol.
D. 0,03 mol và 0,03 mol.
Câu 10: Đốt Fe trong khí clo thiếu thu được hỗn hợp gồm 2 chất rắn. Hãy cho biết thành phần của chất rắn đó:
A. FeCl3 và Fe.
B. FeCl2 và Fe.
C. Fe, FeCl2, FeCl3.
D. FeCl2 và FeCl3.
II. Phần tự luận
Câu 1 (3 điểm): Viết các PTHH xảy ra trong sơ đồ sau:
Câu 2 (2 điểm): Trộn 10,8 gam bột Al với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hoà tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư), thu được 10,752 lít khí H2 (đktc). Tính hiệu suất của phản ứng nhiệt nhôm.
Câu 3 (2 điểm): Cho 4,48 lít khí CO (ở đktc) từ từ đi qua ống sứ đựng 8 gam một oxit sắt đến khi phản ứng xảy ra hoàn toàn. Khí thu được sau phản ứng có tỉ khối so với hiđro bằng 20. Xác định công thức của oxit sắt và phần trăm thể tích của khí CO2 trong hỗn hợp khí sau phản ứng.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| Đ/a | D | B | A | C | D | A | C | D | A | A |
Câu 1:
Chọn đáp án D.
Câu 2: Khi thêm dung dịch axit vào muối cromat màu vàng sẽ tạo thành đicromat có màu da cam. Chọn đáp án B.
Câu 3: M: 1s22s22p63s23p1. Vị trí M trong bảng tuần hoàn là ô 13, chu kì 3, nhóm IIIA. Chọn đáp án A.
Câu 4: Fe tác dụng được với cả 3 dung dịch muối Cu(NO3)2, Fe(NO3)3, AgNO3. Chọn đáp án C.
Câu 5: Câu không đúng: Nhôm là kim loại lưỡng tính. Chọn đáp án D.
Câu 6: Quặng nhôm (nguyên liệu chính) được dùng trong sản xuất nhôm là Boxit Al2O3.2H2O. Chọn đáp án A.
Câu 7: Ta có sơ đồ:
Fe3O4 → 3Fe
232g → 3.56g
x tấn → 800.95% tấn
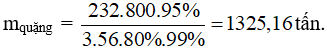
Câu 8: Bảo toàn e: nNO = nCr = 0,1 → V = 2,24 lít. Chọn đáp án D.
Câu 9: Gọi số mol Fe và Mg lần lượt là x và y mol.
Theo bài ra có hệ:
Giải hệ được: x = 0,01 và y = 0,03. Chọn đáp án A.
Câu 10: 2Fe + 3Cl2 → 2FeCl3. Hai chất rắn là FeCl3 và Fe dư. Chọn đáp án A.
2. Phần tự luận
Câu 1 (3 điểm): HS viết đúng mỗi PTHH 0,5 điểm, thiếu cân bằng trừ ½ số điểm mỗi PT
Câu 2 (2 điểm): Tính được: nAl = 0,4 mol, nFe3O4 = 0,15 mol, nH2 = 0,48 mol
Hỗn hợp chất rắn sau phản ứng gồm: Al2O3, Fe, Al dư, Fe3O4 dư
Gọi số mol Al phản ứng là x → số mol Fe = 1,125 mol
Bảo toàn e: (0,4 – x).3 + 1,125x.2 = 0,48.2 → x = 0,32
Giả sử H = 100% → Cả hai chất tham gia phản ứng đều hết
Câu 3 (2 điểm):
Hỗn hợp khí sau phản ứng gồm CO (x mol) và CO2 (y mol)
nhh khí = nCO + nCO2 = nCO bđ → x + y = 0,2 (1)
mhh khí = 20.2.0,2 = 8 gam → 28x + 44y = 8 (2)
Giải hệ được x = 0,05 và y = 0,15 → %VCO2 = 75%.
nCO2 = nO(oxit sắt) = 0,15 mol
mFe(oxit) 8 – 0,15.16 = 5,6 gam → nFe(oxit) = 0,1 mol
Đặt oxit: FexOy → x : y = 0,1 : 0,15 = 2 : 3
Vậy oxit sắt là Fe2O3.
Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Nguồn: /