Đề thi THPT quốc gia năm 2015 môn Hóa Học
Cập nhật: 29/07/2020
1.
Trong các ion sau đây, ion nào có tính oxi hóa mạnh nhất?
A:
Ca2+
B:
Cu2+
C:
Zn2+
D:
Ag+
Đáp án: D
Đáp án đúng là D
2.
Hòa tan hoàn toàn 1,6 gam Cu bằng dung dịch HNO3, thu được x mol NO2 (là sản phẩm khử duy nhất của N+5). Giá trị của x là
A:
0,15
B:
0,05
C:
0,01
D:
0,25
Đáp án: B
Áp dụng bảo toàn mol electron, ta có: ( x = n_{NO_2} = 2.{1,6 over 64} =0,05 mol)
Đáp án đúng B
3.
Cấu hình electron của nguyên tử nguyên tố X là 2s22p63s23p1. Số hiệu nguyên tử của X là
A:
14
B:
27
C:
13
D:
15
Đáp án: C
Đáp án C
4.
Phản ứng nào sau đây không phải là phản ứng oxi hóa – khử?
A:
2KClO3 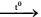 2KCl + 3O2
2KCl + 3O2
B:
2NaOH + Cl2 → NaCl + NaClO + H2O
C:
4Fe(OH)2 + O2 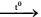 2Fe2O3
2Fe2O3
D:
CaCO3 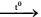 CaO + CO2 + 4H2O.
CaO + CO2 + 4H2O.
Đáp án: D
Lưu ý dùng loại trừ nhanh các phản ứng có đơn chất (trừ 2O3 ⇔ 3O2 ) là phản ứng oxi hóa khử.
Đáp án đúng D
5.
Lưu huỳnh trong chất nào sau đây vừa có tính oxi hóa, vừa có tính khử?
A:
H2SO4.
B:
Na2SO4.
C:
SO2.
D:
H2S.
Đáp án: C
SO2 ( S+4 có thể lên S+6 và xuống S0, S-2).
Đáp án đúng C
6.
Thực hiện các thí nghiệm sau ở điều kiện thường:
(a) Sục khí H2S vào dung dịch Pb(NO3)2.
(b) Cho CaO vào H2O.
(c) Cho Na2CO3 vào dung dịch CH3COOH.
(d) Sục khí Cl2 vào dung dịch Ca(OH)2.
Số thí nghiệm xảy ra phản ứng là
A:
1
B:
4
C:
2
D:
3
Đáp án: B
Các thí nghiệm xảy ra gồm:
(a) H2S + Pb(NO3)2 → PbS(downarrow) HNO + HNO3
(b) CaO + H2O → Ca (OH)2
(c) Na2CO3 + CH3COOH → CHCOO3Na +H2O + CO2
(d) Cl2 + 2Ca(OH)2 → CaCl2 + Ca(OCl)2 + 2H2O
Đáp án đúng là đáp án B
7.
Cho 0,5 gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 0,28 lít H2 (đktc).Kim loại đó là
A:
Mg
B:
Sr
C:
Ba
D:
Ca
Đáp án: D
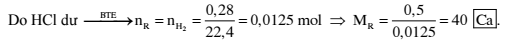
Đáp án đúng là D
8.
Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước?
A:
K
B:
Ba
C:
Na
D:
Be
Đáp án: D
Đáp án đúng là D
9.
Hòa tan hoàn toàn 6,5 gam Zn bằng dung dịch H2SO4 loãng, thu được V lít H2 (đktc). Giá trị của V là
A:
2,24
B:
1,12
C:
3,36
D:
4,48
Đáp án: A
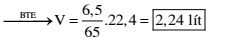
Đáp án đúng A
10.
Kim loại Fe không phản ứng với chất nào sau đây trong dung dịch?
A:
AgNO3
B:
CuSO4
C:
MgCl2
D:
FeCl3
Đáp án: C
Đáp án đúng C
11.
Phương pháp chung để điều chế các kim loại Na, Ca, Al trong công nghiệp là
A:
Thủy luyện.
B:
Điện phân dung dịch.
C:
Nhiệt luyện.
D:
Điện phân nóng chảy.
Đáp án: D
Các kim loại nhóm IA, IIA và Al chỉ được điều chế bằng phương pháp điện phân nóng chảy
Đáp án đúng D
12.
Oxit nào sau đây là oxit axit?
A:
MgO
B:
CrO3
C:
CaO
D:
Na2O
Đáp án: B
Đáp án đúng B
13.
Khử hoàn toàn 4,8 gam Fe2O3 bằng CO dư ở nhiệt độ cao. Khối lượng Fe thu được sau phản ứng là
A:
1,68.
B:
1,44.
C:
2,52.
D:
3,36.
Đáp án: D
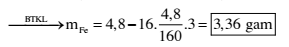
Đáp án đúng D
14.
Quặng boxit được dùng để sản xuất kim loại nào sau đây?
A:
Mg
B:
Al
C:
Cu
D:
Na
Đáp án: B
Đáp án B
15.
Đốt cháy hoàn toàn m gam Fe trong khí Cl2 dư, thu được 6,5 gam FeCl3. Giá trị của m là
A:
2,24
B:
2,80
C:
1,12
D:
0,56
Đáp án: A
 nFe = nFeCl3 = (6,5 over 162,5) = 0,04 mol ⇒ mFe = 0,04 . 56 = 2,24 gam
nFe = nFeCl3 = (6,5 over 162,5) = 0,04 mol ⇒ mFe = 0,04 . 56 = 2,24 gam
Đáp án đúng A
Nguồn: /

