Đề thi thử Đại Học trường THPT Minh Khai -Hà Tĩnh -năm 2014 - Môn Hóa Học
Cập nhật: 12/08/2020
1.
Cho m(g) hỗn hợp X gồm Na, Ca tan hết vào dung dịch Y chứa 0,08 mol NaHCO3 và 0,04 mol CaCl2, sau phản ứng thu được 7 gam kết tủa và thấy thoát ra 0,896 lít khí. Giá trị của m là
A:
1,66 g.
B:
1,72 g
C:
1,2 g
D:
1,56 g
Đáp án: A
Dễ thấy: H2O → OH- + (1 over 2)H2
0,08 0,04
→ HCO3- + OH- → CO32- + H2O
0,08 0,08 0,08
Theo giả thiết thì có 0,07 mol CaCO3 => Ca có 0,03 mol
Na có 0,02 mol => m = 0,02 . 23 + 0,03 . 40 = 1,66 gam
=> Đáp án A
2.
Cho các phản ứng sau trong điều kiện thích hợp
(a) Cl2 + KI dư → (b) O3 + KI dư →
(c) H2SO4 + Na2S2O3 → (d) NH3 + O2 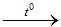
(e) MnO2 + HCl → (f) KMnO4 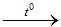
Số phản ứng tạo ra đơn chất là
A:
3
B:
4
C:
5
D:
6
Đáp án: D
Cả 6 phản ứng đều tạo đơn chất.
3.
Một bình kín chứa hỗn hợp X gồm 0,06 mol axetilen; 0,09 mol vinylaxetilen; 0,16 mol H2 và một ít bột Ni. Nung hỗn hợp X thu được hỗn hợp Y gồm 7 hiđrocacbon(không chứa but-1-in) có tỉ khối hơi đối với H2 là( 328 over15). Cho toàn bộ hỗn hợp Y đi qua bình đựng dung dịch AgNO3/NH3 dư, thu được m gam kết tủa vàng nhạt và 1,792 lít hỗn hợp khí Z thoát ra khỏi bình. Để làm no hoàn toàn hỗn hợp Z cần vừa đúng 50 ml dung dịch Br2 1M. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A:
28,71
B:
14,37
C:
13,56
D:
15,18
Đáp án: C
Bảo toàn khối lượng mY = mX = 6,56 (g)
(overline{M_Y}) = (656 over15) => nY = 0,15 mol => nH2phản ứng = 0,16 mol
Gọi x, y là số mol C2H2 và C4H4 đã phản ứng với AgNO3/NH3
- Theo bảo toàn số mol (pi ) => 2x + 3y = 0,06 .2 + 0,09.3 – 0,16 – 0,05 = 0,18 mol. Và x + y = 0,15 – 0,08 = 0,07
x = 0,03 mol; y = 0,04 mol
CAg => CAg 0,03 mol; ; 0,04 mol C4H3Ag. m = 0,03 . 240 + 0,04. 159 = 13,56 (g)
=> Đáp án C
4.
Cho đơn chất lưu huỳnh tác dụng với các chất: O2; H2; Hg; HNO3 đặc, nóng; H2SO4 đặc, nóng trong điều kiện thích hợp. Số phản ứng trong đó lưu huỳnh thể hiện tính khử là
A:
2
B:
3
C:
4
D:
5
Đáp án: B
S thể hiện tính khử khi tác dụng với: O2, HNO3, H2SO4
=> Đáp án B
5.
Thủy phân m (gam) tinh bột trong môi trường axit(giả sử sự thủy phân chỉ tạo glucozo). Sau một thời gian phản ứng, đem trung hòa axit bằng kiềm, sau đó cho tác dụng hoàn toàn với dung dịch AgNO3 trong NH3 dư thu được m (gam) Ag. Hiệu suất của phản ứng thủy phân tinh bột là
A:
66,67%.
B:
80%
C:
75%.
D:
50%
Đáp án: C
(C6H10O5)n → n C6H12O6 → 2nAg. Với h là hiệu suất ta có:
(2mh over 162 ) = (m over 108 ) => h = 75%
=> Đáp án C
6.
Cho 0,896 lít Cl2 hấp thụ hết vào dung dịch X chứa 0,06 mol NaCl; 0,04 mol Na2SO3 và 0,05 mol Na2CO3. Sau khi các phản ứng xẩy ra hoàn toàn thu được dung dịch Y. Cô cạn dung dịch Y thu được m(g) muối khan. Giá trị của m là
A:
21,6g
B:
16,69g
C:
14,93g
D:
13,87g
Đáp án: C
Na2SO3 + Cl2 + H2O → Na2SO4 + 2HCl
0,04 0,04 0,04 0,08
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
0,04 0,08 0,08
=> Dung dịch có: 0,01 mol Na2CO3; 0,04 mol Na2SO4; 0,14 mol NaCl. => m = 14,93 gam
=> Đáp án C
7.
Tiến hành hiđrat hoá 2,24 lít C2H2 với hiệu suất 80% thu được hỗn hợp sản phẩm Y. Cho Y qua lượng dư AgNO3/NH3 thu được m(g) kết tủa. Giá trị của m là
A:
21,6g
B:
23,52g
C:
24 g
D:
22,08g
Đáp án: D
Dễ thấy sản phẩm có: 0,08 mol CH3CHO và 0,02 mol C2H2 => m = 22,08 gam
=> Đáp án D
8.
Cho các chất: Ba; BaO; Ba(OH)2; NaHCO3; BaCO3; Ba(HCO3)2; BaCl2. Số chất tác dụng được với dung dịch NaHSO4 tạo ra kết tủa là
A:
4
B:
5
C:
6
D:
7
Đáp án: C
Chỉ có NaHCO3 không tạo kết tủa
=> Đáp án C
9.
X là một amino axit no (phân tử chỉ có 1 nhóm –NH2 và 1 nhóm -COOH). Cho 0,03 mol X tác dụng với dung dịch chứa 0,05 mol HCl thu được dung dịch Y. Thêm 0,1 mol NaOH vào Y sau phản ứng đem cô cạn thu được 7,895 gam chất rắn. X là
A:
Glixin
B:
Alanin
C:
Valin
D:
Lysin
Đáp án: C
Dễ thấy NaOH dư 0,02 mol => Dung dịch có: 0,02 mol NaOH; 0,05 mol NaCl và 0,03 mol H2N – R-COONa => 0,02. 40 + 0,05. 58,5 + 0,03 . M = 7,895
<=> M = 139 => Mx = 139 – 22 = 117 = Valin
=> Đáp án C
10.
Nung 18,1 gam chất rắn X gồm Al, Mg và Zn trong oxi một thời gian được 22,9 gam hỗn hợp chất rắn Y. Hoà tan hết Y trong dung dịch HNO3 loãng dư được V lít NO(sản phẩm khử duy nhất) và dung dịch chứa 73,9 gam muối. Giá trị của V là
A:
6,72.
B:
3,36
C:
2,24.
D:
5,04
Đáp án: C
Số mol NO3- tạo muối là ((73,9-18,1)over 6)= 0,9mol. Số mol Oxi là 0,3mol
O2- + 2H+ → H2O và NO3- + 4H+ + 3e → NO + 2H2O
0,3 0,6 4a a mol
0,9 + a = 0,6 +4a → a = 0,1mol → V = 2,24lit
=> Đáp án C
11.
Chất hữu cơ X có công thức phân tử C9H12. Khi cho X tác dụng với clo có mặt bột sắt hoặc tác dụng với clo khi chiếu sáng đều thu được 1 dẫn xuất monoclo duy nhất. Tên gọi của X là
A:
Cumen
B:
Propylbenzen
C:
1-etyl-3-metylbenzen
D:
1,3,5-trimetylbenzen
Đáp án: D
1, 3, 5 – Trimetylbenzen.
=> Đáp án D
12.
Trộn V(ml) dung dịch H3PO4 0,08M với 250 ml dung dịch NaOH 0,32M dư thu được dung dịch X chứa 2 chất tan có cùng nồng độ mol. Giá trị của V là
A:
250 ml
B:
2000 ml
C:
(2000 over 3)ml
D:
400 ml
Đáp án: A
Do NaOH dư
H3PO4 + 3NaOH → Na3PO4 + 3H2O
x 3x x.
=> 0,08 – 3x = x <=> x = 002 mol => V = 250 ml
=> Đáp án A
13.
Thuỷ phân hoàn toàn 0,1 mol 1 péptít X (mạch hở, được tạo bởi các (alpha)- amino axit có 1 nhóm –NH2 và 1 nhóm -COOH) bằng dung dịch HCl vừa đủ thu được dung dịch Y. Cô cạn dung dịch Y thu được chất rắn có khối lượng lớn hơn khối lượng của X là 52,7 gam. Số liên kết péptít trong X là
A:
14
B:
9
C:
11
D:
13
Đáp án: B
Gọi x là số liên kết peptit của X. 1 mol X sẻ phản ứng với x mol H2O và (x + 1) mol HCl. Ta có: 0,1x .18 + 0,1(x + 1). 36,5 =52,7 ⇔ x = 9
=> Đáp án B
14.
Ion M3+ có cấu hình e của khí hiếm Ne. Vị trí của M trong bảng hệ thống tuần hoàn là
A:
Chu kỳ 2, nhóm VIIIA
B:
Chu kỳ 2, nhóm VA
C:
Chu kỳ 3, nhóm IIIA
D:
Chu kỳ 3, nhóm IVA
Đáp án: C
Ne ( Z = 10) => M(Z = 13)
=> Đáp án C
15.
Hỗn hợp X gồm 2 axit no. Đốt cháy hoàn toàn a mol hỗn hợp X thu được a mol H2O. Mặt khác, cho a mol hỗn hợp X tác dụng với NaHCO3 dư thu được 1,4 a mol CO2. % khối lượng của axit có khối lượng mol nhỏ hơn trong X là
A:
26,4%
B:
27,3%
C:
43,4%
D:
35,8%
Đáp án: C
Đốt a mol X được a mol H2O → Htb = 2. Dễ thấy 2 axit là HCOOH và (COOH)2. Chọn a = 1 => x + y = 1; x + 2y = 1,4. => HCOOH 0,6 mol; (COOH)2 0,4 mol => %HCOOH = 43,4%
=> Đáp án C
Nguồn: /

