Khái quát về nhóm Nito
Cập nhật: 01/07/2020
Vị trí các nhóm Nito trong ban tuần hoàn :
Nhóm nitơ gồm các nguyên tố: nitơ (N), photpho (P), asen (As), antimon (Sb) và bitmut (Bi). Chúng đều thuộc các nguyên tố p.
Bảng 2.1. Một số tính chất của các nguyên tố nhóm nitơ
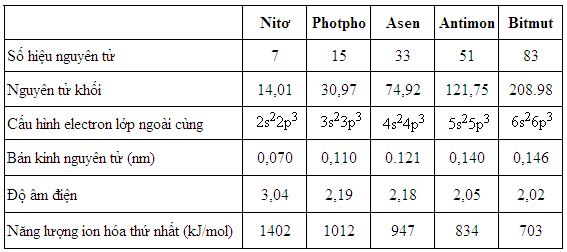
Tính chất chung của các nguyên tố nhóm Nito :
+) Cấu hình electron nguyên tử
Lớp electron ngoài cùng của nguyên tử là ns2np3 (có 5 electron)
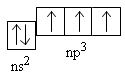
Ở trạng thái cơ bản, nguyên tử của các nguyên tố nhóm nitơ có 3 electron độc thân, do đó trong một số hợp chất chúng có hóa trị 3.
Đối với nguyên tử của các nguyên tố P,As,Sb và Bi ở trạng thái kích thích, một electron trong cặp electron của phân lớp ns có thể chuyển sang obitan d trống của phân lớp nd.
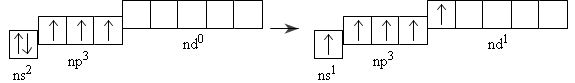
Như vậy, ở trạng thái kích thích nguyên tử của các nguyên tố này có 5 electron độc thân nên có thể có hóa trị năm trong các hợp chất.
+) Sự biến đổi tính chất của các đơn chất
- Tính oxi hóa - khử
Do đó khả năng giảm và tăng số oxi hóa trong các phản ứng hóa học, nên nguyên tử các nguyên tố nhóm nitơ thể hiện tính oxi hóa và tính khử. Khả năng oxi hóa giảm dần từ nitơ đến bimut, phù hợp với chiều giảm độ âm điện của nguyên tử các nguyên tố trong nhóm.
Nguồn: /

